多发性骨髓瘤患者静脉血栓栓塞的预防与治疗:欧洲骨髓瘤网络临床实践指南
时间:2025-09-07 12:09:56 来源 网络 作者:网络
静脉血栓栓塞(VTE)是多发性骨髓瘤(MM)患者中常见的严重并发症,发生率显著高于普通人群。VTE包括深静脉血栓(DVT)、肺栓塞(PE)以及不典型血栓(如脑静脉或肠系膜静脉血栓)。MM患者VTE的发生率为每年每1000人年8至22例,且与显著的发病率、死亡率、治疗中断和生活质量下降相关。VTE风险由MM特异性因素(如高凝状态、免疫调节剂[IMiD]、内皮功能障碍)和患者相关因素共同驱动。
为了促进MM患者的最佳管理,欧洲骨髓瘤网络(EMN)组织跨学科专家小组制定了MM患者VTE预防与治疗的实践指南,该指南遵循PICO(人群、干预、对照、结果)格式。近日发表于《HemaSphere》。

关键建议包括
-
患者教育:向患者普及VTE风险及深静脉血栓和肺栓塞的体征和症状。
-
专门化护理:建立专门的诊断和治疗路径,针对门诊中发生的VTE进行管理。
-
风险评估:定期使用经过验证的评分系统评估VTE风险。
-
一级预防:对高危患者启动低分子肝素(LMWH)或直接Xa因子抑制剂(anti-Xa药物)的药物预防。
-
及时诊断和治疗:早期诊断VTE并立即使用LMWH或anti-Xa药物进行抗血栓治疗。
-
二级预防:根据患者VTE复发风险或出血风险的个体特征,制定长期抗血栓治疗方案。

MM患者的一级血栓预防
与VTE相关的风险因素
识别VTE高风险患者对于在MM患者中有效和安全地使用药物血栓预防至关重要。应在诊断时、复发时以及系统治疗期间评估患者的VTE风险。必须将患者分为VTE高危和中/低危,从而实现靶向预防策略,平衡药物血栓预防的获益与潜在的出血风险。
VTE的预测因子已从基于人群的数据库、登记库、医院记录、回顾性队列、前瞻性观察研究和临床试验中确定。
总体风险受以下因素影响:
i. 疾病相关风险因素。 MM与高凝状态和内皮细胞活化有关。诊断后的时间(NDMM患者比复发患者VTE风险更高,因为肿瘤负荷通常在初始诊断时最高)、肿瘤负荷、 固定(immobilization;由于骨病或任何其他原因)、副蛋白血症的水平和类型是MM相关血栓形成的预测因子。单克隆副蛋白血症可能导致高粘滞血症、高纤维蛋白原血症、天然凝血抑制剂蛋白C或蛋白S活性降低、获得性活化蛋白C抵抗或纤溶受损。细胞因子如白细胞介素-6和肿瘤坏死因子(TNF),以及浆细胞来源的细胞外囊泡,可导致内皮细胞活化和血小板活化;所有这些都与VTE风险相关。
ii. 抗骨髓瘤治疗。IMiDs(沙利度胺、来那度胺和泊马度胺,以及iberdomide和mezigdomide)会增加VTE风险。接受沙利度胺或来那度胺单药治疗的患者VTE发生率为3%-4%。加用大剂量地塞米松或多药化疗,VTE风险增加至26%。尽管减少地塞米松剂量可降低VTE风险,但其风险仍较高,约为10%。此外,高VTE风险与治疗暴露时间无关。与来那度胺相比,泊马度胺相关的VTE风险较低,据报道,接受4mg剂量的患者VTE发生率在3%至7%之间,且呈剂量依赖性。使用蛋白酶体抑制剂硼替佐米治疗与低VTE风险相关。卡非佐米诱导高凝状态并与VTE风险增加相关。在一项纳入924名接受卡非佐米/来那度胺/地塞米松(KRd)治疗的患者的荟萃分析中,VTE发生率为8.9%,而在1380名接受硼替佐米/来那度胺/地塞米松(VRd)治疗的患者中为6.2%。该研究回顾了一项随机试验和五项回顾性研究,但仅有两项研究使用了预先指定的风险评估工具进行VTE风险评估,Piedra等人使用了SAVED-VTE风险评分,而Loncharich等人使用IMPEDE评分对患者进行分层。在一项回顾性研究(n=672)中,接受KRd治疗的患者VTE发生率为10.6%,接受达雷妥尤单抗-来那度胺-地塞米松加蛋白酶体抑制剂治疗的患者为8.9%,接受VRd治疗的患者为7%。在Piedra等人的研究(n=305)中,接受KRD加阿司匹林(ASA)的患者VTE发生率为16.1%,接受KRD加利伐沙班的患者为4.8%,接受VRD加ASA的患者为4.8%。CARDAMON试验报告称,接受卡非佐米-环磷酰胺-地塞米松治疗的患者中有2.8%发生血栓性微血管病。在EMN09研究中,不含IMiD的卡非佐米-苯达莫司汀-地塞米松联合方案的VTE发生率为10%。抗CD38单克隆抗体达雷妥尤单抗和其他单克隆抗体,如belantamab mafodotin或elotuzumab,以及口服蛋白酶体抑制剂伊沙佐米,尚未发现会放大血栓形成风险。在GRIFFIN研究中,将达雷妥尤单抗联合VRD(D-VRd)与VRd进行比较,所有级别的累积VTE发生率分别为10%和15%。根据方案,抗血栓预防按照IMWG指南进行,80%的患者接受乙酰水杨酸,15%接受LMWH,5%-8%接受直接Xa因子抑制剂。对III期CASTOR、POLLUX和MAIA试验的事后汇总分析表明,达雷妥尤单抗治疗并未增加VTE风险。双特异性抗体与VTE风险增加无关。一项对47项研究的荟萃分析,纳入了7040名接受CAR T细胞治疗的血液恶性肿瘤(包括MM)患者,显示在CAR T细胞给药后的前6个月内,VTE的总体发生率为2.4%,而任何出血事件的发生率为1.9%。动脉血栓形成的发生率在0.3%至0.8%之间。
iii. 患者相关的内在风险因素。 高龄(尤其是70岁以上的患者)、女性、个人VTE史、存在已知的遗传性血栓形成倾向(因子V Leiden或因子II G20210A突变、抗凝血酶、蛋白C或蛋白S缺乏)或其他基因多态性(即ABO基因座)、心血管风险因素(糖尿病、肥胖、高血压和血脂异常)或心血管疾病(缺血性卒中、冠状动脉或颈动脉疾病以及外周动脉疾病)、炎症性肠病、自身免疫性疾病和肾功能不全,是癌症相关血栓形成(CAT)最常见和最重要的风险因素之一。
iv. 触发风险因素。 中心静脉导管、使用促红细胞生成素或其他集落刺激因子、近期住院(少于3个月)或因急性内科疾病住院、免疫抑制、外科手术干预和固定(任何原因)是MM患者VTE的主要触发风险因素。
MM患者VTE的风险评估模型
个体化VTE风险评估以确定应接受药物血栓预防的患者,是一项临床需求,正如ESMO癌症患者VTE预防和治疗临床实践指南(ESMO Clinical Practice Guideline for the Prevention and Treatment of VTE in Cancer Patients)所推荐的那样。国际骨髓瘤工作组(IMWG)、EMN和国家综合癌症网络(NCCN)发布的指南采用了一种自2014年以来在实践中使用的简化算法,该算法基于IMiD为基础的治疗是VTE风险的主要决定因素的概念。然而,该算法并非源于推导队列分析,而是基于对VTE风险预测因子的经验性评分。根据IWMG算法,患者被分为两个风险组:低危(0-1个风险因素)和危险(≥2个风险因素)(表2)。IWMG风险分层并不准确,导致VTE风险被低估。临床研究和病例系列系统地记录了“低危”组患者的高VTE发生率。
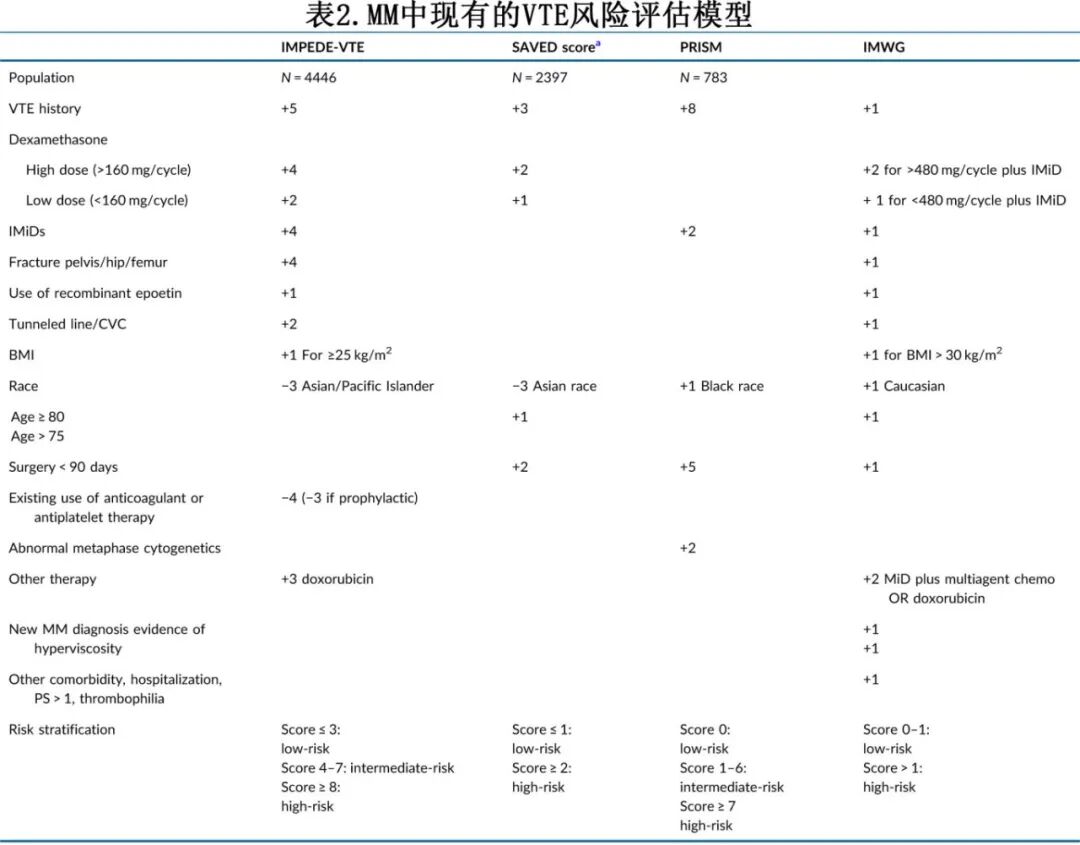
为了改进MM中的VTE风险分层,出现了三种经过验证的评分系统:IMPEDE-VTE、SAVED和PRISM(表2和表3)。这些工具代表了风险预测方面的重大进步,但每种工具都有不同的临床应用和局限性。
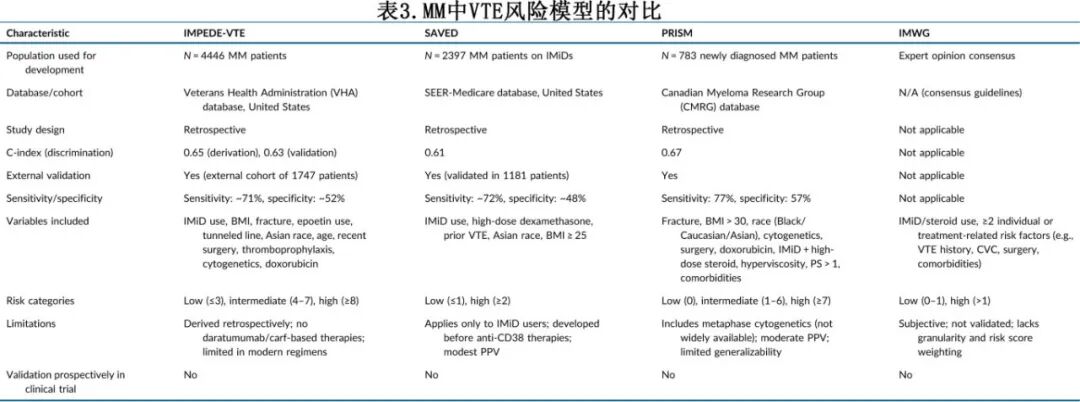
IMPEDE-VTE评分源自对退伍军人管理局癌症登记处回顾性数据库(包括4446名患者)的分析,并在SEER-Medicare数据库中进行了验证。IMPEDE-VTE评分将患者分为低、中、高危组,6个月随访的VTE发生率分别为3.3%、8.3%和15.2%。与IMWG/NCCN模型(c-statistic = 0.55)相比,IMPEDE-VTE评分显示出更好的预测准确性(c-statistic = 0.64)。IMPEDE-VTE评分源自未经选择的真实世界MM人群,使其广泛适用于各种临床场景——包括新诊断的未接受过化疗的患者、正在接受积极骨髓瘤治疗的患者以及疾病进展或复发的患者。这种普遍性源于其在异质性队列中的开发,没有限制性的入组标准。
SAVED评分源自对SEER-Medicare数据库中可获得的2397名接受IMiDs治疗的患者进行的回顾性数据库分析(表2和表3)。SAVED评分的适用性固有地仅限于接受IMiDs的患者,因为其推导队列完全由接受IMiD治疗的患者组成。SAVED评分将患者分为VTE低危和高危。与IMWG/NCCN模型(c-statistic = 0.55)相比,SAVED评分的预测准确性略高(c-statistic = 0.6)。
PRISM评分源自克利夫兰诊所治疗的934名患者的回顾性数据库,将患者分为低、中、高危组(表2和表3),12个月VTE发生率分别为2.7%、10.8%和36.5%。在哥伦比亚大学欧文医学中心的一组257名患者中对PRISM评分进行的外部验证显示预测准确性较低(c-statistic为0.59),尽管与IMWG/NCCN算法(c-statistic = 0.55)相比略有改善。
与IMWG/NCCN算法相比,IMPEDE-VTE、SAVED和PRISM评分代表了在识别有VTE风险的MM患者方面的重要进步,因为它们源自明确定义的队列并经过验证。
总之,三种评分的比较(表2)突出了几个重要点:
i.IMPEDE-VTE和PRISM评分可应用于任何MM患者,而SAVED评分专门为接受IMiD治疗的患者设计。
ii. PRISM评分的适用性因其依赖于中期细胞遗传学评估而受到限制,而中期细胞遗传学并非常规进行。此外,由于该评分源自单中心队列研究,其普遍性受到质疑。
所有模型的常见局限性和观点
所有当前的风险评估模型(RAM)均源自回顾性队列,这些队列主要包含接受较老治疗方案(主要是双药方案)的患者,而非现在MM患者标准的三联或四联方案。此外,IMPEDE-VTE和SAVED评分的推导队列大多涉及接受高地塞米松(≥160 mg/周期)的患者,这不再被认为是标准治疗。新药如卡非佐米和达雷妥尤单抗在这些数据集中代表性不足或完全缺失。
鉴于这些局限性,需要通过在接受新型抗骨髓瘤治疗的患者队列中评估它们来更新或重新校准RAM,还需要提高评分的预测准确性。最后,当前临床评分的阳性预测值仍然不高(大约15%),突出表明需要更精确的分层工具。纳入特定的高凝状态生物标志物为提高评分准确性,特别是阳性预测值,提供了一个有前景的策略。正在进行的前瞻性研究正在评估生物标志物的临床效用,如D-二聚体、凝血酶生成、促凝磷脂依赖性凝血时间、P-选择素水平和循环促凝微囊泡,以及内皮细胞活化标志物。将这些经过临床验证的生物标志物与既定的临床RAM相结合,有望提高MM患者VTE风险评估的准确性和可靠性。
在目前可用的VTE风险评估评分中,IMPEDE-VTE评分满足评估所有MM患者的最低标准,因为它全面包含相关风险因素,适用于各种治疗方案,依赖于主要可用的临床预测因子,并且与IMWG/NCCN或SAVED或PRISM评分相比具有更好的准确性。
血栓预防策略
旨在评估MM患者一级药物血栓预防有效性和安全性的临床试验有限。
目前的IMWG指南推荐低剂量ASA用于低危MM患者的血栓预防。来自临床研究的累积证据表明,与LMWH相比,ASA对VTE的保护作用较差,在IMiD治疗人群中,相对风险(RR)降低分别约为50% versus 70%-80%。然而,鉴于其既定的安全性特征和潜在获益,低剂量阿司匹林对于VTE低危MM患者来说仍然是一个合理的血栓预防选择。一项对439名门诊MM患者进行的荟萃分析显示,与维生素K拮抗剂(VKAs)相比,使用LMWH进行血栓预防显著降低了症状性VTE的风险(RR 0.33, 95% CI 0.14-0.83;高确定性证据)。在781名患者中,与ASA相比,LMWH显著降低了症状性VTE的发生率(RR 0.51, 95% CI 0.22-1.17;2项研究,中等确定性证据)。在接受LMWH或VKA治疗的患者中未观察到严重出血,在接受ASA治疗的患者中报告率低于1%。
一项更近期的系统评价仅确定了四项随机临床试验(RCT),总共包括1042名患者,评估了MM患者药物血栓预防的有效性和安全性。两项研究比较了低剂量ASA与预防性LMWH。一项研究评估了VKA与LMWH或ASA,第四项研究比较了低剂量ASA与直接抗Xa药物;比较ASA、VKA和LMWH有效性和安全性的证据确定性为低至极低。这种不确定性可能源于用于患者分层和分配血栓预防方案的风险评估模型的准确性有限。这些方法学上的缺陷可能导致研究间的高度异质性,并且无法证明一种干预措施明显优于另一种。
一项系统文献综述确定了10项RCT和观察性研究,纳入接受直接抗Xa药物或ASA进行一级血栓预防的MM患者(n=1026)。与ASA相比,使用直接抗Xa药物进行血栓预防的VTE发生率较低(优势比[OR] 0.33;95% CI 0.16-0.68;P < 0.001),而两组之间的出血事件没有显著差异。作者建议谨慎,因为人群特征的异质性和所纳入观察性研究的潜在偏倚。一项对MM患者研究的探索性荟萃分析调查了使用ASA与无干预或预防剂量LWMH的血栓预防。分析了10项研究的1964名患者。在几项纵向研究和两项RCT中,与无干预相比,ASA显著降低了VTE风险(OR = 0.20;95% CI: 0.07-0.61;P = 0.005;I2=41%),但与LMWH相比,VTE风险更高(OR = 2.60;95% CI: 1.08-6.25;P = 0.03;I2=0%)。一项较早的前瞻性观察研究(MELISSE试验)招募了接受IMiDs治疗的MM患者,报告接受ASA的患者VTE发生率为7%,而接受LMWH治疗的患者为3%,接受VKA治疗的患者为0。
在MM门诊患者中使用直接抗Xa药物进行血栓预防是一个有吸引力的策略,因为其给药方式方便,治疗窗宽,并且与VKA相比药物相互作用有限。AVERT和CASSINI试验分别将574名和841名CAT中/高危患者(基于Khorana风险评分值≥2)随机分配到安慰剂组或阿哌沙班2.5 mg每日两次或利伐沙班10 mg每日一次组。在AVERT试验中,使用阿哌沙班2.5 mg每日两次持续180天与比安慰剂更低的VTE发生率相关(4.2% vs. 1.2%;HR: 0.41 [95% CI 0.26-0.65; P = 0.0001];需治疗人数 = 17)。阿哌沙班组患者的严重出血率更高(3.5% vs. 1.8%;HR 2.00 [95% CI 1.01-3.95; P = 0.046];需伤害人数 = 59)。在CASSINI试验中,给予利伐沙班10 mg每日一次持续180天并未显示与安慰剂相比VTE风险有显著差异。但是,在治疗期间分析中,利伐沙班的VTE发生率显著较低(2.6% vs. 6.4% HR 0.40 [95% CI 0.2-0.8])。两组的严重出血率均较低且相当。两项研究均未纳入严重血小板减少症(血小板计数 <50 ×109/L)或严重肾功能损害(肌酐清除率[CrCl] <30 mL/min)的患者。值得注意的是,这些研究中仅纳入有限数量的MM患者。三项初步研究和一项回顾性研究纳入MM患者,并显示使用阿哌沙班2.5 mg每日两次进行至少6个月血栓预防的有效性和安全性的有希望的结果。在305名患者中,仅报告了两起VTE事件(0.6%)。一项对305名NDMM患者的回顾性研究表明,使用利伐沙班10 mg每日一次进行血栓预防可能是一种有效且安全的手段。在接受KRD加利伐沙班治疗的患者中,VTE发生率为4.8%,而接受ASA治疗的患者为16.1%,与接受VRD和ASA治疗的患者相似(4.8%)。一项小型研究对37名NDMM或复发疾病患者比较了使用华法林(剂量调整至国际标准化比值[INR]达到2-3)或阿哌沙班2.5 mg每日两次进行3个月血栓预防的有效性和安全性。华法林组未观察到VTE事件。阿哌沙班组报告了一例VTE事件,严重出血事件分别发生在两名和四名患者中。另一项针对70名接受基于IMiD方案的NDMM患者的研究报告称,在接受阿哌沙班2.5 mg每日两次的患者中未发生VTE病例,但发生两起动脉事件和一起严重出血事件,凸显了在该患者群体中持续评估抗凝策略的必要性。总体而言,数据表明直接抗Xa药物与LWMH相比具有同等的有效性和安全性,证明了在这种情况下使用任何一种药物的合理性。
尽管如此,仍需要进行III期RCT来评估在高危MM患者中使用直接抗Xa药物或LMWH进行血栓预防的有效性和安全性。
血栓预防的持续时间
随着MM患者生存率的提高,需要更加关注VTE风险的长期管理。NDMM患者在诱导治疗后接受长期来那度胺维持治疗,复发患者继续治疗直至疾病进展或出现不可接受的毒性。因此,需要定期评估延长药物血栓预防的获益-风险比。来那度胺维持治疗具有持续的VTE风险,介于4%和6%之间。对Griffin试验的事后分析显示,VTE风险在诱导期最高,但随着时间的推移持续增加(达雷妥尤单抗-VRd在7-18周期维持期间为2.2%,VRd为7%;在18周期以上维持期间分别为3.6%和1.7%)。在后续治疗线中,即使肿瘤负荷减少,VTE风险仍然存在。
优化MM患者长期药物血栓预防获益-风险比的关键步骤包括:
i. 实施经过验证的RAM(例如,IMPEDE-VTE)并定期重新评估VTE风险。
ii. 考虑治疗特异性风险(IMiDs、高剂量地塞米松等)。
iii. 定期重新评估血栓/出血风险
• 评估出血风险预测因子:贫血、血小板减少症、肾功能和肝功能以及药物间相互作用。
iv. 定期评估患者的偏好、患者的依从性以及长期血栓预防对生活质量指标的影响。
v. 以下方面的患者教育
•早期识别VTE的症状和体征,
•早期识别出血素质的症状和体征
•在发生出血或VTE时明确的患者路径。
建议
-
建议向MM患者提供有关VTE的教育材料,应包括关于VTE负担及其在MM患者中的后果、VTE的风险因素、VTE的临床体征和症状、提高患者意识的指导以及与专门管理VTE和抗血栓治疗的医生沟通的信息(1A)。
-
建议对所有MM患者在初始诊断、治疗开始、复发/进展以及修改方案时实施系统性的VTE风险评估(1A)。
-
建议在所有MM患者中实施IMPEDE-VTE评分进行VTE风险评估;鉴于其全面包含相关风险因素、适用于各种治疗方案以及依赖于普遍可用的临床参数。IMPEDE-VTE评分应在其局限性的背景下应用(1B)。
-
建议将患者分为两个风险组:VTE高危/中危或低危(2A)。
-
接受基于IMiD的方案或卡非佐米联合治疗的患者应分层为VTE高危/中危(2B)。
-
建议在初次诊断和抗骨髓瘤治疗开始时、诱导完成或疾病缓解后、诊断疾病进展或复发时、计划修改治疗方案时进行VTE风险评估(2B)。
-
建议对归类为VTE高危/中危的患者使用直接抗Xa药物或LMWH进行药物血栓预防(1B)。
a. 建议用于高危/中危MM患者血栓预防的抗血栓药物包括(剂量指南见表4):
i. LMWH,每日一次皮下注射,使用卫生当局批准的预防剂量并按照说明书推荐。
ii. 利伐沙班 10 mg 每日一次口服。
iii. 阿哌沙班 2.5 mg 每日两次口服。
iv. 建议考虑将阿哌沙班2.5 mg每日两次或利伐沙班10 mg每日一次作为CrCl > 30 mL/min、对LMWH有禁忌症或不耐受或有肝素诱导的血小板减少症病史的患者的潜在替代方案。对于CrCl < 30 mL/min的患者,LMWH(如果需要,调整剂量)是首选预防方案(2B)。
v.如果直接抗Xa药物不可用且LMWH有禁忌症,VKAs也可作为选择(剂量调整至目标INR为2.0-3.0)。

-
建议对计划进行药物血栓预防的VTE高危/中危患者评估出血风险(考虑血小板计数、血红蛋白水平、肾功能、抗凝禁忌症、药物间相互作用以及个人临床相关出血史)(1A)。
-
建议对归类为低危的患者使用低剂量阿司匹林(2B)。
-
建议自最后一次风险评估起至少应用药物血栓预防6个月。专家小组不鼓励停止血栓预防,特别是在接受IMiD治疗的有残留疾病的患者中。在维持治疗期间,是否降级血栓预防措施应基于每个具体案例进行考虑。这需要通过IMPEDE评分进行风险评估,并仔细权衡利弊比,同时考虑患者个人的偏好以及药物血栓预防对患者生活质量的影响。
-
专家小组鼓励对使用LMWH或直接抗Xa药物进行血栓预防的有效性和安全性进行研究,并进行基于风险分层患者选择的III期研究。
-
专家小组鼓励对现有RAM进行比较研究,并进行适当设计的前瞻性队列研究,以推导和验证临床生物学RAM,从而准确识别有资格接受血栓预防的MM患者。
急性内科疾病MM患者的血栓预防
患有急性内科疾病(包括COVID-19)的MM患者同样受益于急性内科疾病患者的标准血栓预防实践,并应接受最新指南中推荐的相同血栓预防。
建议
-
建议对活动性MM和急性内科疾病患者,无论是住院还是在初级医疗机构或家中接受护理,均给予预防剂量的LMWH或磺达肝癸钠(1A)。
MM患者VTE的治疗
近20年来,LMWH一直是恶性肿瘤患者血栓形成急性期和长期二级预防的首选。在CAT患者中进行的III期RCT表明,直接抗Xa药物阿哌沙班、艾多沙班或利伐沙班与LMWHs相比具有相似的有效性和安全性。
多中心随机双盲非劣效性试验APICAT比较了在1766名活动性肿瘤和近端DVT或PE并已完成至少6个月抗凝治疗的患者中,使用减少剂量(2.5 mg)或全剂量(5.0 mg)阿哌沙班每日两次治疗12个月(2.5 mg 每日两次)的有效性和安全性。MM患者在减少剂量组中占3.8%,在全剂量组中占4.1%。中位治疗持续时间为11.8个月。减少剂量组有18名患者发生复发性VTE(累积发生率,2.1%),全剂量组有24名(累积发生率,2.8%)(调整后亚分布HR, 0.76; 95% CI, 0.41 - 1.41; P = 0.001 非劣效性)。减少剂量组有102名患者发生临床相关出血(累积发生率,12.1%),全剂量组有136名(累积发生率,15.6%)(调整后亚分布HR, 0.75; 95% CI, 0.58 - 0.97; P = 0.03)。减少剂量组的死亡率为17.7%,全剂量组为19.6%(调整后HR, 0.96; 95% CI, 0.86 - 1.06)。对于活动性肿瘤患者,延长减少剂量阿哌沙班抗凝在预防复发性VTE方面不劣于全剂量阿哌沙班。减少剂量导致临床相关出血并发症的发生率低于全剂量。
MM患者在上述临床试验中代表性不足,但总体而言,VTE管理遵循与其他恶性肿瘤相同的模式。
在特定患者(即老年和体弱患者、肾功能不全患者和肝功能不全患者)中,与直接抗Xa药物相比,使用LMWH治疗具有根据体重或皮下注射后4小时测量的血浆抗Xa活性水平调整剂量的优势。与直接抗Xa药物相比,LMWH治疗具有根据体重或皮下注射后4小时测量的血浆抗Xa活性水平调整剂量的优势。此外,LMWH的药物相互作用较少,这一点在患者正在接受细胞色素P450 3A4(CYP3A4)和P-糖蛋白的强效抑制剂或诱导剂治疗时尤其重要。
对于肾功能不全的MM患者,用于VTE二级预防的抗血栓治疗的安全性尚无数据。事后和亚组分析表明,对于中度肾功能不全(CrCl 30-60 mL/min)的患者,LMWH和直接Xa因子抑制剂可以在不调整剂量的情况下给药,因为安全性和有效性特征不会改变。严重肾功能不全(CrCl < 30 mL/min)的患者被排除在随机III期临床试验之外,并且缺乏在该情况下使用抗Xa药物的数据。因此,应使用普通肝素(UFH)随后改用VKA,或使用根据抗Xa活性水平调整剂量的LMWH。对于严重血小板减少症(<50×109/L)的患者,如果血栓进展风险高,可以在血小板输注支持下进行全剂量抗凝,或者对于风险较低的情况,中等或预防剂量的LMWH可作为选择。
浅静脉血栓形成的最佳管理尚未确立,且缺乏MM患者的数据。长隐静脉距隐股交界处(SFJ)3厘米内的浅静脉血栓形成(SVT)被认为等同于DVT。对于较不严重的SVT形式,建议至少进行6周的治疗性抗凝,然后转为预防,但缺乏MM特异性数据来指导临床实践。
建议
-
MM患者VTE急性期的治疗。
1.建议在开始抗血栓治疗前系统评估出血风险。出血风险的预测因素包括:肾功能不全、低血小板计数(<50 G/L)、贫血和药物间相互作用(对于直接抗Xa药物)(1A)。
2.在不中断抗骨髓瘤治疗的情况下,建议
a. 对高出血风险患者开始治疗剂量的LMWH(1A);
b. 对低出血风险和低药物间相互作用潜力的患者开始治疗剂量的阿哌沙班、edoxaban或利伐沙班(edoxaban需要在前5-10天使用LMWH进行引导治疗)(1A);
c. 对严重肾功能不全(CrCl < 30 mL/min)的患者开始治疗剂量的UFH,并定期监测血浆中的抗Xa水平(1A)。
3.建议在基于IMiD/卡非佐米的治疗方案期间发生危及生命或复发性VTE的情况下,进行个体化治疗决策。个体化治疗策略中需要考虑的因素包括对当前治疗方案的缓解深度、血栓事件的严重程度以及患者的复发性VTE风险特征(2C)。
-
MM患者VTE的二级预防。
1.建议LMWH或抗Xa药物(阿哌沙班、艾多沙班或利伐沙班)用于VTE二级预防(1A)。
a. 应根据肾功能和潜在的药物间相互作用选择最佳的抗血栓药物(1B)。
2.建议对患有VTE和MM的患者进行至少6个月的抗血栓治疗(1A)。
• 活动性MM定义为 (i) NDMM, (ii) 复发/进展的MM, (iii) 尽管接受治疗但未缓解的MM疾病。
3.建议对活动性MM患者将抗血栓治疗延长至6个月以上(1A)。
4.建议对持续接受IMiD或卡非佐米治疗的患者将抗血栓治疗延长至6个月以上。
5.建议对于活动性MM患者,关于将抗血栓治疗延长至6个月以上的决策应涉及仔细评估VTE复发风险与出血风险(等级1A)。
a. 建议将患者转诊给血栓和止血专家。在长期抗血栓治疗期间,有必要定期重新评估血栓和出血风险(2B)。
6. 对于MM患者,若需要在索引事件后6个月进行长期二级预防血栓治疗,建议使用减量的阿哌沙班(2.5mg,每日两次)而非全剂量的阿哌沙班(5mg,每日两次)。(1B)。
导管相关VTE的预防和治疗
在肿瘤患者中证据稀少,且没有MM特异性的数据。有一项前瞻性试验评估了LMWH加VKA在癌症患者导管相关VTE中的效果。关于Xa因子抑制剂的作用尚无可靠数据。
建议
-
不推荐常规药物预防用于预防导管相关VTE(2C)。
-
对于MM患者有症状的导管相关VTE,推荐抗凝治疗至少3个月(2A)。首选的一线治疗是LMWH,但抗Xa药物或VKAs可作为替代选择(2C)。
-
建议对MM患者有症状的导管相关VTE进行至少3个月的抗血栓治疗,抗凝(等级2A)。首选的一线治疗是LMWH,直接口服抗Xa药物或VKAs可作为替代选择(2C)。
-
建议在抗血栓治疗3个月后评估骨髓瘤相关VTE的风险,如果患者被分层为高危/中危,则应用推荐的血栓预防(2C)。
-
总体而言,无法推断出进一步的MM特异性建议。专家小组建议这些患者按照非MM患者的标准临床实践进行管理,并鼓励设计能够提供关于MM患者使用CVC数据的试验。
讨论
EMN-VTE共识指南标志着MM患者VTE管理方面的重大进步。这些建议是通过在EMN主持下,血栓形成专家和MM专家之间严密的多学科合作制定的。该专家共识提供了个体化的、基于证据的策略,以解决骨髓瘤病理生理学及其治疗所固有的独特血栓形成风险。
本文档引入了关键更新,包括通过将中危和高危患者分组来简化风险分层,并主张将Xa因子抑制剂与LMWH一起用于一级血栓预防。专家小组推荐对所有新诊断或复发开始接受IMiDs或卡非佐米联合治疗的患者进行普遍的抗血栓预防,无论基线风险评分如何,前提是经过仔细的出血风险评估。该建议得到了数据的支持,数据显示接受IMiDs的患者即使按风险模型分层,VTE发生率仍然持续较高,并且认识到当前的风险评估模型是在卡非佐米使用之前开发的。通过将疾病活动性和当代治疗方案整合到其框架中,EMN-VTE指南解决了未满足的临床需求,并旨在协调和改进真实世界的血栓预防实践。
专家小组共识指南阐述的关键点如下:
1.VTE是MM常见且危及生命的并发症,对患者的生活质量产生负面影响,干扰预定治疗,并降低预期寿命。
2.血液学家、血管学家、血栓和止血专家以及全科医生应做到以下几点:
• 告知患者VTE的风险,教育他们了解临床体征和症状,靶向可改变的风险因素,并告知他们及时诊断和治疗的途径。
• 通过应用推荐的RAM进行常规和定期的VTE风险评估,承认这些评分的准确性欠佳。
• 定期评估出血风险,承认目前尚无经过验证的用于符合药物血栓预防条件的门诊癌症患者的出血风险RAM。
• 对于中危和高危患者,使用LMWH或Xa因子抑制剂(阿哌沙班或利伐沙班)以推荐的预防剂量启动药物血栓预防。
• 对归类为低危的患者启动低剂量ASA。
• 对所有即将开始基于IMiD或卡非佐米治疗的患者,使用LMWH或Xa因子抑制剂(阿哌沙班或利伐沙班)以推荐的预防剂量启动药物血栓预防。
• 药物血栓预防应至少持续6个月,之后进行个案评估。
• 预先确定一个本地医疗路径——从初级医疗机构到专门的学术中心——以便对门诊MM患者进行VTE的及时诊断和治疗。
• 对确诊VTE的患者,使用治疗剂量的LMWH或Xa因子抑制剂启动抗血栓治疗,至少持续6个月。
• 对于索引事件后6个月有资格进行VTE长期二级预防的患者,优先选择低剂量阿哌沙班2.5 mg每日两次,优于全剂量阿哌沙班(5 mg每日两次)。
• 应用个性化策略进行VTE二级预防的长期抗凝,需考虑疾病状态、血液学反应和出血风险。
• 选择最佳抗血栓药物,无论是用于一级血栓预防还是VTE治疗,都应考虑患者的偏好、对生活质量的影响以及药物间相互作用。
鉴于管理MM患者的复杂性,无论是有VTE风险还是已确诊VTE,加之疾病进展的动态性、不断演变的治疗方案以及人口老龄化,专家小组强烈建议建立专门的门诊血栓咨询。需要更有效和更新的VTE风险评估工具,这些工具应基于包含三联/四联新型药物组合的队列进行前瞻性开发,以准确反映当前的临床实践。此外,需要前瞻性随机试验来回答基于MM特异性患者特征的最佳血栓预防方式和持续时间的问题。VTE很可能仍然是MM患者持续存在的风险,作为一个团体,我们需要实施一致的临床实践以改善临床结局。
参考文献
Gerotziafas, G., Fotiou, D., Nijhof, I., Ay, C., Lecumberri, R., Laroca, A., Cook, G., Engelhardt, M., Zweegman, S., Delforge, M., Maraveyas, A., Lefkou, E., Marchetti, M., Van de Donk, N.W.C.J., Gay, F., Ludwig, H., Einsele, H., San Miguel, J.F., Dimopoulos, M.A., Boccadoro, M., Sonneveld, P., Falanga, A. and Terpos, E. (2025), Prevention and treatment of venous thromboembolism in patients with multiple myeloma: Clinical practice guidelines on behalf of the European Myeloma Network. HemaSphere, 9: e70177. https://doi.org/10.1002/hem3.70177


